Teilbereich 1: Altern von Stammzellen
Die Forschungsgruppen innerhalb des Teilbereichs 1 untersuchen die Ursachen und Folgen der Stammzellalterung. Die Forschungsarbeit erstreckt sich von Modellorganismen über genetische Mausmodelle bis hin zu Mausmodellen, die mit menschlichen Stammzellen angereichert sind.
Mit der Schließung von zwei Gruppen in 2016 ist die Stammzellforschung an Wirbellosen-Modellen im Teilbereich 1 reduziert. Das Institut geht davon aus, dass mit der Rekrutierung neuer Gruppen diese Lücke geschlossen warden kann.
Die Forschung ist durch vier Schwerpunkte definiert:
- Zellintrinsische Mechanismen, die die Funktion alternder Stamm- und Vorläuferzellen einschränken,
- Alternsbedingte Veränderungen der Stammzellnischen und des systemischen Umfelds,
- Mechanismen der klonalen Selektion und epigenetische Drifts bei der Stammzellalterung und
- Mikrobiota- und stoffwechselbedingte Beeinträchtigungen der Stammzellfunktion während des Alterns (im Zusammenhang mit dem neuen Schwerpunkt Mikrobiota und Altern, der ím Teilbereich 2 aufgebaut wird).
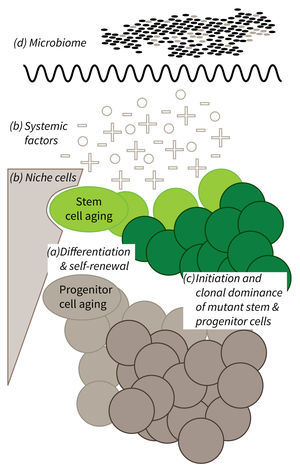
Forschungsfokus von Teilbereich 1.
a) Derzeit ist noch nicht vollständig bekannt, welche Mechanismen die Zellfunktionen im Alter beeinträchtigen. b) Der relative Einfluss von Nischenzellen und systemisch wirkenden Faktoren auf die Stammzellalterung müssen für verschiedene Gewebe noch erforscht werden. c) Die klonale Ausbreitung mutanter Zellen wird mit der Entstehung von Krankheiten im Alter in Verbindung gebracht. Mechanistisch ist der Prozess jedoch noch kaum verstanden. Die Veränderungen in der Farbintensität stehen für die klonale Dominanz von ursprünglichen Stamm- (grün) und Vorläuferzellen (grau). d) Es gibt zunehmend Hinweise darauf, dass alternsbedingte Veränderungen im Mikrobiom die Stammzellfunktion beeinflussen und vice versa.
Publikationen
(seit 2016)
2017
- The use of urinary proteomics in the assessment of suitability of mouse models for ageing.
Nkuipou-Kenfack E, Schanstra JP, Bajwa S, Pejchinovski M, Vinel C, Dray C, Valet P, Bascands JL, Vlahou A, Koeck T, Borries M, Busch H, Bechtel-Walz W, Huber TB, Rudolph KL, Pich A, Mischak H, Zürbig P
PLoS One 2017, 12(2), e0166875 - Activated protein C protects from GvHD via PAR2/PAR3 signalling in regulatory T-cells.
Ranjan S, Goihl A, Kohli S, Gadi I, Pierau M, Shahzad K, Gupta D, Bock F, Wang H, Shaikh H, Kähne T, Reinhold D, Bank U, Zenclussen AC, Niemz J, Schnöder TM, Brunner-Weinzierl M, Fischer T, Kalinski T, Schraven B, Luft T, Huehn J, Naumann M, Heidel FH, Isermann B
Nat Commun 2017, 8(1), 311 - Mitochondrial BAX Determines the Predisposition to Apoptosis in Human AML.
Reichenbach F, Wiedenmann C, Schalk E, Becker D, Funk K, Scholz-Kreisel P, Todt F, Wolleschak D, Döhner K, Marquardt** JU, Heidel** F, Edlich** F
Clin Cancer Res 2017, 23(16), 4805-16 ** co-corresponding authors - Macrophage's little helper: vitamin A directs alternatively activated monocyte-derived macrophages to tissue-resident macrophages.
Schlüter D, Heidel FH
Cell Mol Immunol 2017, 14(10), 805-8 - Cell autonomous expression of CXCL-10 in JAK2V617F-mutated MPN.
Schnöder TM, Eberhardt J, Koehler M, Bierhoff HB, Weinert S, Pandey AD, Nimmagadda SC, Wolleschak D, Jöhrens K, Fischer T, Heidel FH
J Cancer Res Clin Oncol 2017, 143(5), 807-20 - Hoxa9 activation by epigenetic alterations in aging muscle stem cells induces developmental signals impairing regeneration of aging muscle
Schwörer S
Dissertation 2017, Jena, Germany - Wnt activity and basal niche position sensitize intestinal stem and progenitor cells to DNA damage.
Tao S, Tang D, Morita Y, Sperka T, Omrani O, Lechel A, Sakk V, Kraus J, Kestler HA, Kühl M, Rudolph KL
EMBO J 2017, 36(19), 2920-1 Erratum for EMBO J 2015 volume 34 page 624 - Synergistic killing of FLT3ITD-positive AML cells by combined inhibition of tyrosine-kinase activity and N-glycosylation.
Tsitsipatis D, Jayavelu AK, Müller JP, Bauer R, Schmidt-Arras D, Mahboobi S, Schnöder TM, Heidel F, Böhmer FD
Oncotarget 2017, 8(16), 26613-24 - Nicotinamide adenine dinucleotide replenishment rescues colon degeneration in aged mice.
Zhu X, Shen W, Wang Y, Jaiswal A, Ju Z, Sheng Q
Signal Transduct Target Ther 2017, 2, 17017