Jena. Jedes Lebewesen ist von Mikroben besiedelt – Pilze, Bakterien, Archaeen und Viren. Zusammen bilden sie das Mikrobiom. Das Mikrobiom des Menschen setzt sich aus Billionen Mikroorganismen zusammen. Sie besiedeln Haut und Schleimhäute und bilden gegenüber Krankheitserregern eine stoffwechselaktive Barriere, die für die Gesundheit essenziell ist. Dabei ist die Zusammensetzung des Mikrobioms bei jedem Menschen einzigartig, und sie verändert sich abhängig von äußeren Einflüssen wie Ernährung, Infektionen oder durch Kontakt mit anderen Menschen. Aber das Mikrobiom verändert sich auch dadurch, dass wir altern. Das Ökosystem, das der Mensch als Wirtsorganismus zusammen mit den Mikroben bildet, kann, so wie andere Ökosysteme auch, aus dem Gleichgewicht geraten.
Balance des Ökosystems Mensch-Mikrobe ist im Alter gefährdet
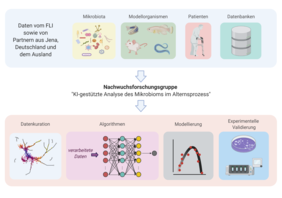
„Wenn das Mikrobiom im Darm seine Diversität einbüßt (d. h. weniger unterschiedliche Arten von Mikroorganismen aufweist) und von wenigen Spezies dominiert wird, dann gesellen sich typischerweise Krankheitserreger hinzu. Sie sind eine Gefahr für die Gesundheit des Wirts. Infektionen und entzündliche Prozesse werden wahrscheinlicher und lösen eine Kaskade von Reaktionen aus, die sich negativ auf die Funktion zahlreicher Organe wie Leber und Gehirn auswirken. Und das passiert eher bei älteren Menschen“, sagt Prof. Dario R. Valenzano, der am Leibniz-Institut für Alternsforschung - Fritz-Lipmann-Institut (FLI) in Jena die Forschungsgruppe „Evolutionsbiologie / Mikrobiom-Wirt-Interaktionen beim Altern“ leitet. Der Evolutionsbiologe will gemeinsam mit seinem Kollegen am FLI, dem Bioinformatiker Prof. Steve Hoffmann neue Wege gehen, um zu verstehen, wie dieser Zusammenbruch des Ökosystems Mensch-Mikrobe zu Krankheiten führt. Wie verhalten sich die Billionen Mikroben zueinander und wie im Austausch mit den Körperzellen? Dafür richtet das FLI 2022 eine neue Nachwuchsforschungsgruppe namens „KI-gestützte Analyse des Mikrobioms im Alternsprozess“ ein. Die Carl-Zeiss-Stiftung fördert das Vorhaben im Rahmen ihres Themenschwerpunkts Künstliche Intelligenz mit 2,5 Mio. Euro über fünf Jahre.
Neue Methoden für die Vorhersage von Krankheiten
Die neue Forschungsgruppe wird Verfahren des maschinellen Lernens und der künstlichen Intelligenz entwickeln und anwenden, um aus biologischen Daten neue Erkenntnisse zu gewinnen. Ziel ist es, mithilfe einer Kombination verschiedener Methoden der Datenanalyse Modelle zu entwickeln, die Aussagen zum Krankheits- und Gesundheitszustand auf Grundlage der Zusammensetzung des Mikrobioms erlauben.
„Solche Methoden könnten in der Zukunft verstärkt bei der Diagnose von Darmkrebs oder chronisch-entzündlichen Darmerkrankungen zum Einsatz kommen“, sagt Steve Hoffmann, der am FLI den Forschungsbereich „Systembiologie und Bioinformatik des Alterns“ leitet. „KI-basierte Methoden können uns auch dabei helfen, Veränderungen in der Zusammensetzung und der Funktion der Mikrobiom-Bestandteile im Zeitverlauf zu analysieren. Diese zeitliche Dimension ist uns natürlich die wichtigste, schließlich altern wir nur mit der Zeit“, betont Hoffmann.
Die Daten, um solche KI-basierten Vorhersagemodelle zu „trainieren“, haben Wissenschaftlerinnen und Wissenschaftler am FLI seit Jahrzehnten generiert. Dazu zählen beispielsweise Langzeit-Datenreihen zum Transkriptom (also der Gesamtheit der Gene, die in einer Zelle transkribiert werden) während des Alterns, sowie Daten zum Einfluss des Mikrobioms auf epigenetische Veränderungen und Daten zur Zusammensetzung von Stuhlproben, die Fischen und Mäusen im Laufe ihres Lebens entnommen wurden.
Mehr Erkenntnisse durch bessere Analyse von Forschungsdaten
„Die Einbeziehung der Methoden des maschinellen Lernens in die Mikrobiomforschung und die Alternsforschung bedeutet eine enorme Steigerung des Erkenntnisgewinns, der aus komplexen Datensammlungen gezogen werden kann“, sagt Prof. Alfred Nordheim, Wissenschaftlicher Direktor des FLI. „Wir sind der Carl-Zeiss-Stiftung für die Unterstützung dieser wichtigen Entwicklung am FLI sehr dankbar.“
Kontakt
Kristina Vaillant
Managerin Kommunikation
Tel.: 03641-65-6373
E-Mail: presse@~@leibniz-fli.de