Teilbereich 1: Altern von Stammzellen
Die Forschungsgruppen innerhalb des Teilbereichs 1 untersuchen die Ursachen und Folgen der Stammzellalterung. Die Forschungsarbeit erstreckt sich von Modellorganismen über genetische Mausmodelle bis hin zu Mausmodellen, die mit menschlichen Stammzellen angereichert sind.
Mit der Schließung von zwei Gruppen in 2016 ist die Stammzellforschung an Wirbellosen-Modellen im Teilbereich 1 reduziert. Das Institut geht davon aus, dass mit der Rekrutierung neuer Gruppen diese Lücke geschlossen warden kann.
Die Forschung ist durch vier Schwerpunkte definiert:
- Zellintrinsische Mechanismen, die die Funktion alternder Stamm- und Vorläuferzellen einschränken,
- Alternsbedingte Veränderungen der Stammzellnischen und des systemischen Umfelds,
- Mechanismen der klonalen Selektion und epigenetische Drifts bei der Stammzellalterung und
- Mikrobiota- und stoffwechselbedingte Beeinträchtigungen der Stammzellfunktion während des Alterns (im Zusammenhang mit dem neuen Schwerpunkt Mikrobiota und Altern, der ím Teilbereich 2 aufgebaut wird).
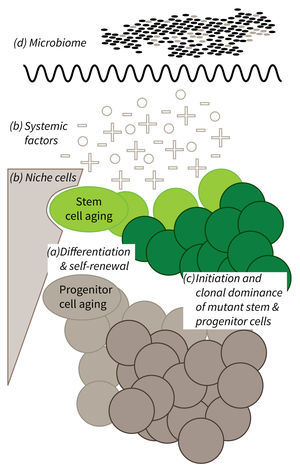
Forschungsfokus von Teilbereich 1.
a) Derzeit ist noch nicht vollständig bekannt, welche Mechanismen die Zellfunktionen im Alter beeinträchtigen. b) Der relative Einfluss von Nischenzellen und systemisch wirkenden Faktoren auf die Stammzellalterung müssen für verschiedene Gewebe noch erforscht werden. c) Die klonale Ausbreitung mutanter Zellen wird mit der Entstehung von Krankheiten im Alter in Verbindung gebracht. Mechanistisch ist der Prozess jedoch noch kaum verstanden. Die Veränderungen in der Farbintensität stehen für die klonale Dominanz von ursprünglichen Stamm- (grün) und Vorläuferzellen (grau). d) Es gibt zunehmend Hinweise darauf, dass alternsbedingte Veränderungen im Mikrobiom die Stammzellfunktion beeinflussen und vice versa.
Publikationen
(seit 2016)
2023
- Resident and recruited macrophages differentially contribute to cardiac healing after myocardial ischemia
Weinberger T, Messerer D, Joppich M, Fischer M, Garcia C, Kumaraswami K, Wimmler V, Ablinger S, Räuber S, Fang J, Liu L, Han Liu W, Winterhalter J, Lichti J, Tomas L, Esfandyari D, Percin G, Martin Salamanca S, Hidalgo A, Waskow C, Engelhardt S, Todica A, Zimmer R, Pridans C, Gomez-Perdiguero E, Schulz C
bioRxiv 2023, 10.1101/2023.05.08.539799
2022
- Vitamin A metabolism in niche cells activates retinoic acid signaling and impairs stem cell function and skeletal muscle maintenance in aging mice
Becker F
Dissertation 2022, Jena - Impaired formation of neutrophil extracellular traps (NETs) in patients with myelodysplastic syndrome.
Brings C, Fröbel J, Cadeddu RP, Germing U, Haas R, Gattermann N
BLOOD ADV 2022, 6(1), 129-37 - Combined Activity of the Redox-Modulating Compound Setanaxib (GKT137831) with Cytotoxic Agents in the Killing of Acute Myeloid Leukemia Cells.
Demircan MB, Mgbecheta PC, Kresinsky A, Schnoeder TM, Schröder K, Heidel FH, Böhmer FD
Antioxidants (Basel) 2022, 11(3) - Context-specific effects of NOX4 inactivation in acute myeloid leukemia (AML).
Demircan MB, Schnoeder TM, Mgbecheta PC, Schröder K, Böhmer FD, Heidel FH
J Cancer Res Clin Oncol 2022, 148(8), 1983-90 - Histone demethylase KDM4C is a functional dependency in JAK2-mutated neoplasms.
Ernst P, Schnöder TM, Huber N, Perner F, Jayavelu AK, Eifert T, Hsu CJ, Tubío-Santamaría N, Crodel CC, Ungelenk M, Hübner CA, Clement JH, Hochhaus A, Heidel FH
Leukemia 2022, 36(7), 1843-9 - Muscle stem cell maintenance and regeneration of skeletal muscle require functional motor innervation
Henze H
Dissertation 2022, Jena, Germany - Taz protects hematopoietic stem cells from an aging-dependent decrease in PU.1 activity.
Kim* KM, Mura-Meszaros* A, Tollot* M, Krishnan MS, Gründl M, Neubert L, Groth M, Rodriguez-Fraticelli A, Svendsen AF, Campaner S, Andreas N, Kamradt T, Hoffmann S, Camargo FD, Heidel FH, Bystrykh LV, de Haan G, von Eyss B
Nat Commun 2022, 13(1), 5187 * equal contribution - Meeting Report: Aging Research and Drug Discovery
Meron E, Thaysen M, Angeli S, Antebi A, Barzilai N, Baur JA, Bekker-Jensen S, Birkisdottir M, Bischof E, Bruening J, Brunet A, Buchwalter A, Cabreiro F, Cai S, Chen BH, Ermolaeva M, Ewald Collin Y, Ferrucci L, Florian MC, Fortney K, Freund A, Georgievskaya A, Gladyshev VN, Glass D, Golato T, Gorbunova V, Hoejimakers J, Houtkooper RH, Jager S, Jaksch F, Janssens G, Borch Jensen M, Kaeberlein M, Karsenty G, de Keizer P, Kennedy B, Kirkland JL, Kjaer M, Kroemer G, Lee KF, Lemaitre JM, Liaskos D, Longo VD, Lu YX, MacArthur MR, Maier AB, Manakanatas C, Mitchell SJ, Moskalev A, Niedernhofer L, Ozerov I, Partridge L, Passegué E, Petr MA, Peyer J, Radenkovic D, Rando TA, Rattan S, Riedel CG, Rudolph L, Ai R, Serrano M, Schumacher B, Sinclair DA, Smith R, Suh Y, Taub P, Trapp A, Trendelenburg AU, Valenzano DR, Verburgh K, Verdin E, Vijg J, Westendorp RGJ, Zonari A, Bakula D, Zhavoronkov A, Scheibye-Knudsen M
Aging (Albany NY) 2022, 14(2), 530–543 - Characterization of Novel α-Mangostin and Paeonol Derivatives With Cancer-Selective Cytotoxicity.
Nunna S, Huang YP, Rasa M, Krepelova A, Annunziata F, Adam L, Käppel S, Hsu MH, Neri F
Mol Cancer Ther 2022, 21(2), 257-70